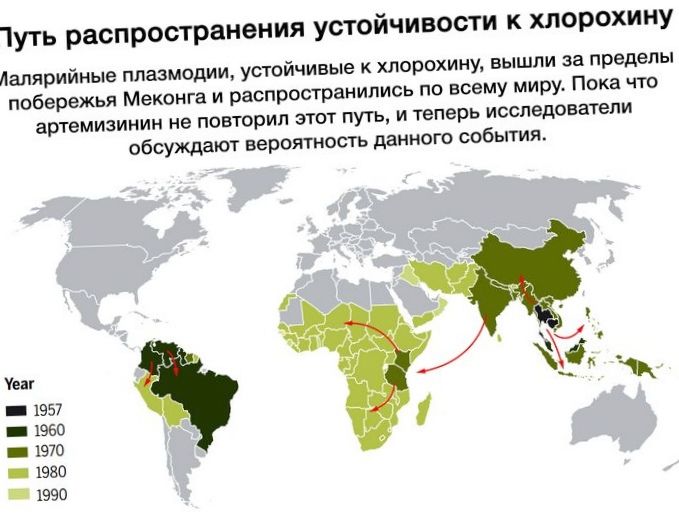
От малярии каждый год погибает около 3 миллионов людей. По большей части ей болеют в Африки, в Южной и Юго-Восточной Азии, а также в государствах Латинской Америки.
Химиотерапия, благодаря которой возможно убить малярийный плазмодий, действенна, но существуют 2 неприятности. Во-первых, паразитическое простейшее весьма скоро производит устойчивость к лекарственным средствам. Во-вторых, у малярийного плазмодия сложный жизненный цикл, и особи на различных его стадиях имеют различную чувствительность к применяемым препаратам. Так, кое-какие виды плазмодия, вызывающие ovale- и vivax-малярию (т.е.
Plasmodium ovale и Plasmodium vivax), передавая клетки печени, впадают в них в «спячку», в следствии чего спустя некое время по окончании казавшегося исцеления наступает рецидив – заболевание возвращается, поскольку «дремлющий» паразит просыпается.
К сожалению, пока вакцины от малярии не существует, исходя из этого химиотерапия есть единственным способом лечения, что, но, всё чаще и чаще терпит неудачу.
Однако, благодаря сочетанию современных способов органического синтеза, молекулярной биологии и скрининга, группе учёных, объединивших исследователей из Америки, Индии, Англии, Канады, Австралии, японии и Голландии удалось отыскать молекулу, которая высоко активна в отношении многих стадий жизненного цикла малярийного плазмодия и владеет хорошими фармакокинетическими чертями, что делает её хорошим кандидатом для испытаний.
Одним из продуктивных походов к созданию лекарственных средств есть скрининг – определение активности огромного числа соединений, образующих так именуемую библиотеку. Для наработки библиотеки применяют реакции, на протяжении которых вероятно ровное образование солидного числа сходных соединений с разными помощниками.
Стратегию современного подхода к созданию библиотек возможно обрисовать словами, каковые на русский возможно перевести как «строй, соединяй, замыкай» (build-couple-pair). Сущность этого подхода в следующем. На первом этапе («строй») синтезируют строительные блоки которые содержат хиральные центры и пара функциональных групп либо реакционных центров, дабы их возможно было применять на следующих стадиях. На второй стадии («соединяй») разнородные строительные блоки вводят в реакцию между собой.
В заключении подвергают оказавшиеся соединения (так именуемые конъюгаты) внутримолекулярной циклизации (стадия «замыкай»), внутримолекулярно связывая реакционные центры и функциональные группы.
По окончании того, как библиотека взята, нужно прогнать её через скрининговое решето, т.е. отделить активные молекулы от неактивных. В этом случае было не одно решето, а пара. Первое пропускало молекулы, каковые были активны в отношении эритроцитарной формы лекарственно устойчивого штамма самый опасного вида малярийного плазмодия Plasmodium falciparum, вызывающего так именуемую тропическую малярию.
Эритроцитарная стадия – это стадия развития малярийного плазмодия, на которой он фактически и приводит к симптомам заболевания. Как раз её прежде всего и нужно лечить.
Вещества испытывали в концентрации 10 мкМ (10 микромолей на литр). Из 100 000 соединений через это решето смогло пройти около 1500 молекул.
Принципиально важно отметить следующее.
На сегодня существует пара классов противомалярийных агентов, действующих на различные молекулярные мишени паразита. В случае если плазмодий устойчив к одному препарату класса, то с высокой возможностью он будет устойчив и к остальным препаратам этого класса. Исходя из этого в подобного рода скрининговых изучениях принципиально важно отсеять те новые молекулы, каковые действуют на уже узнаваемые мишени.
С целью этого прошедшие первичный скрининг молекулы испытывали на штаммах плазмодия, устойчивых к применяемым препаратам, дабы не изобретать заведомо бракованный велосипед.
Потом с отобранными молекулами трудились следующим образом.
Во-первых, контролировали их на активность в отношении экзоэритроцитарной (внеэритроцитарной) печёночной формы паразита (тканевых шизонтов). Вещества испытывали в 4 концентрациях. Отбор проходили те, для которых EC50 3 мкМ (концентрация, при которой ингибировалось развитие 50 % шизонтов) и СС5040 мкМ (концентрация, при которой погибало 50 % клеток печени).
Не считая тканевых шизонтов, каковые передают клетки печени в инкубационный период, и эритроцитарной стадии, на которой появляется характерный симптом малярии – перемежающаяся лихорадка, существуют ещё и гаметоциты – стадия половых клеток. Это так называемая трансмиссивная стадия, поскольку как раз гаметоциты попадают в здорового малярийного комара, если он выпьет крови больного малярией человека.
Уничтожение гаметоцитов не облегчит страдания больного, но будет серьёзным бонусом в борьбе с распространением малярии, поскольку обрывает путь её передачи от больного к переносчику. Вот из-за чего на 2 стадии скрининга молекул удостоверились в надежности кроме этого на активность в отношении гаметоцитов.
Так что же в итоге?
В следствии всех этих мытарств было найдено соединение, которое in vitro (т.е. в стекле, в пробирке) было деятельно в отношении 3 жизненных форма паразита: эритроцитарных и тканевых шизонтов, и гаметоцитов. Структура данной няшки (BRD3444) такова:
Как осознать, на что действует эта молекула?
Для этого исследователи решили вывести устойчивого к ней плазмодия и взглянуть, как изменился его геном. Зная, мутация каких участков ДНК случились, возможно выяснить, за синтез каких белков они отвечают. Так и сделали. Оказалось, что новоиспечённая молекула ингибирует фенилаланин-тРНК-синтетазу – фермент, что пришпандоривает аминокислоту фенилаланин к транспортной РНК, дабы последняя имела возможность наращивать полипептидную цепочку белка.
Точности для отмечу, что при выяснении механизма действия трудились не с отысканной путём скрининга молекулой, а с её более растворимым аналогом, в котором гидроксильная несколько заменена на аминогруппу.
Что дальше?
А дальше – это основное.
Как я писал, BRD3444 владеет одним недочётом – она не отлично растворяется в воде. Но это не самый ответственный её недочёт. BRD3444 весьма скоро метаболизируется, что ведет к низкой длительности судьбы молекулы в организме и требует нередкого приёма.
Так, соединение потребовало доработки.
Как осознать, какие конкретно части молекулы возможно трогать без утраты активности, а какие конкретно – нет? В этот самый момент сильно помогла выбранная стратегия синтеза «строй, соединяй, замыкай». Одной из её изюминок есть то, что она направлена на получение стереоизомеров – молекул, отличающихся пространственным размещением атомов в пространстве.
Те из вас, кто знаком с базами стереохимии, легко выяснят, что для BRD3444 вероятно существование 8 стереоизомеров. По окончании изучения их биологической активности оказалось, что конфигурация 2 из 3 асимметрических атомов углерода очень важна для сохранения высокой активности в отношении малярийного плазмодия. Конфигурация третьего асимметрического центра была не столь серьёзна: оба диастереомера, отличающиеся по его конфигурации, были высоко активны.
Это навело на идея, что манипуляции с помощниками именно у этого атома углерода наименее всего будут сказываться на активности молекулы. Так и выяснилось.
Достаточно простые манипуляции разрешили взять соединение, которое задерживается в организме мыши значительно продолжительнее и, помимо этого, владеет пара большей активностью – BRD7929. Данный улучшенный аналог владел активностью в отношении всех 3 стадий жизненного цикла плазмодия, видящегося в организмах млекопитающих: эритроцитарных и тканевых шизонтов, и гаметоцитов. Одной его дозы хватало как для профилактики, так и исцеления заражённых животных.
Кстати, весьма интересно, как новейшие технологии разрешают проводить скрининг с минимальными упрочнениями. Не могу не написать об этом.
Хороший способ определения наличия плазмодия – микроскопия мазов крови. Способ достаточно чувствительный и не весьма трудоёмкий. Но, сами осознаёте, в то время, когда у тебя в опыте много грызунов, микроскопия и взятие крови преобразовываются в тяжёлый труд, да и крови у небольших грызунов, мышей, не всегда очень наберёшься, в особенности в случае если нужно следить за течением заболевания пара недель. на данный момент за ваш счёт доступно фактически любое наслаждение.
К примеру, в обрисованном мною изучении паразитемию, т.е. число плазмодиев в крови, определяли посредством особого прибора по биолюминисценции. Мышку посветили светом, а позже взглянули, как она сама светится: чем посильнее, тем больше в крови паразитов. Лепота!
Ну и пара критических замечаний, дабы оправдать иронию заголовка моего рассказика.
В опытах по определению мишени для происхождения устойчивости к новому классу соединений малярийному плазмодию пригодилась всего 1 мутация в гене, кодирующем фенилаланин-тРНК-синтетазу. Не обращая внимания на то, что происхождение таковой мутации маловероятно, заняло продолжительное время и потребовало постепенного повышения концентрации терапевтического агента, пройдёт несколько годков по окончании того, как препараты этого класса покажутся в клинике, – и всей птичке пропасть: мутантный плазмодий продолжит, как ни в чём не бывало, кушать гемоглобин отечественных с вами эритроцитов.
Появляется пара вопросов к токсичности открытого класса потенциальных противомалярийных препаратов. Не обращая внимания на то, что отобранное на протяжении скрининга соединение BRD3444 не владело цитотоксичностью, умеренная цитотоксичность свойственна его производным. Помимо этого, кое-какие из этих производных возможно смогут проявлять кардиотоксичность.
Необычно кроме этого, что медицинские химики, каковые трудились над проектом, в упор не увидели возможности образования страшных хинонимнов… Что-то мне подсказывает, что путь аналогов BRD3444 в клинику будет непростым. Захотим им удачи.
Благодарю за внимание.
ДИАНА ШУРЫГИНА — КОНЕЦ ИСТОРИИ (ПУСТЬ ГОВОРЯТ)
Интересные записи на сайте:
- Наса сделало фотографии ударной звуковой волны на фоне солнца
- Перед проверкой скорости интернета
- Составлена карта взаимодействий генов дрожжей
- Установлено строение вируса зика
- Страны снг выбирают модель управления инновациями
Подобранные по важим запросам, статьи по теме:
-
Удивительная история черных дыр: конец звездной судьбы
Научное мышление подчас конструирует объекты со столь парадоксальными особенностями, что кроме того самые проницательные ученые сначала отказывают им в…
-
Ученые совершили революционный прорыв в лечении малярии
Научный прорыв может проложить путь к появлению новых способов лечения малярии, заявляют исследователи. По словам ученых, их открытие может привести к…
-
60 лет назад принято Распоряжение о постройке космодрома Плесецк Само собой разумеется, в то время никто не имел возможности предположить, какое значение…
-
20010,0,3500, В этом обзоре мы представим материалы для организаторов туристско-экскурсионной работы по будущей эко трассе Николаев-Ольвия-Очаков. Как…
-
Успех тв: ольга гершензон об истории и планах итц «сканэкс»
Успех ТВ: Время громадных географических открытий сзади. Эра космоса началась более полувека назад. Но появляются всё новые и более идеальные разработки,…
-
Тайная правда о самых громких загадках в истории человечества
10 октября — Всем людям нравятся загадки. Мы любим истории о Джеке Потрошителе, Филадельфийском опыте, пропавшем Бермудском треугольнике и боинге — так…